FDA widzi potencjał w polskim projekcie od Urteste. Test Panuri na drodze do rejestracji
Polski projekt Panuri, rozwijany przez spółkę Urteste, może stać się przełomem w diagnostyce nowotworowej. Dzięki innowacyjnej technologii badania enzymów w próbkach moczu, rozwiązanie to pozwala na wykrycie raka na etapie przedinwazyjnym, znacznie zwiększając szanse pacjentów na skuteczne leczenie. Spółka już wykazała wysoką skuteczność testu oraz przedstawiła obiecujące wyniki wstępnych konsultacji z amerykańską FDA. Przygotowuje się do badania klinicznego, na które finansowanie ma już zapewnione.
Flagowy projekt Panuri
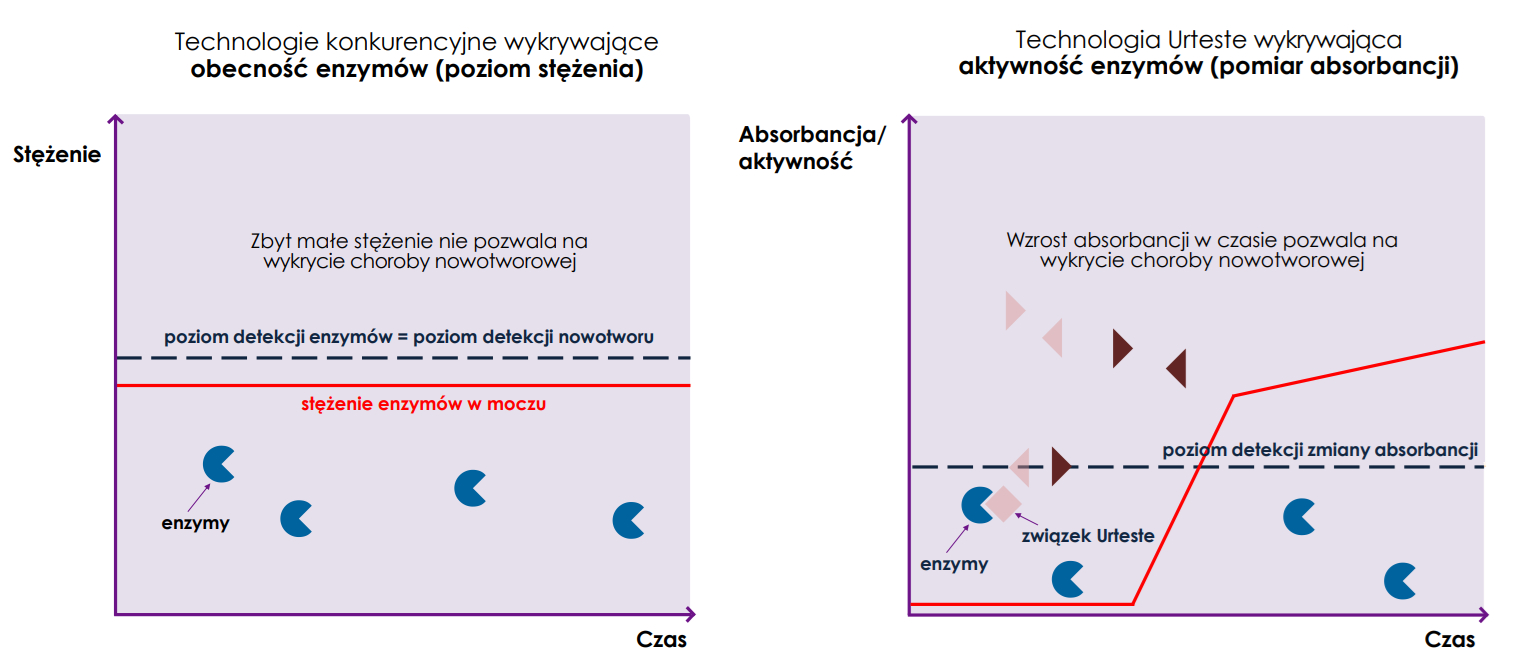
Projekt odpowiada na potrzebę medyczną, którą jest wczesne wykrywanie raka, zanim stanie się on trudny do leczenia lub wręcz niemożliwy. Przesuwa więc wykrycie nowotworu na okres przedinwazyjny i tym samym zwiększa znacząco szansę na usunięcie nowotworu.
„Szukamy aktywności enzymatycznej enzymów poprzez dodanie do próbki moczu opracowanego przez nas związku chemicznego, który przy połączeniu z enzymem daje sygnał widzialny dla urządzeń, które stosujemy. Nasza technologia pozwala więc zauważać te enzymy, dać sygnał, który jest z diagnostycznego punktu widzenia, dowodem na to, że rozwija się w organizmie choroba nowotworowa” – wyjaśnia Tomasz Kostuch, założyciel członek zarządu.
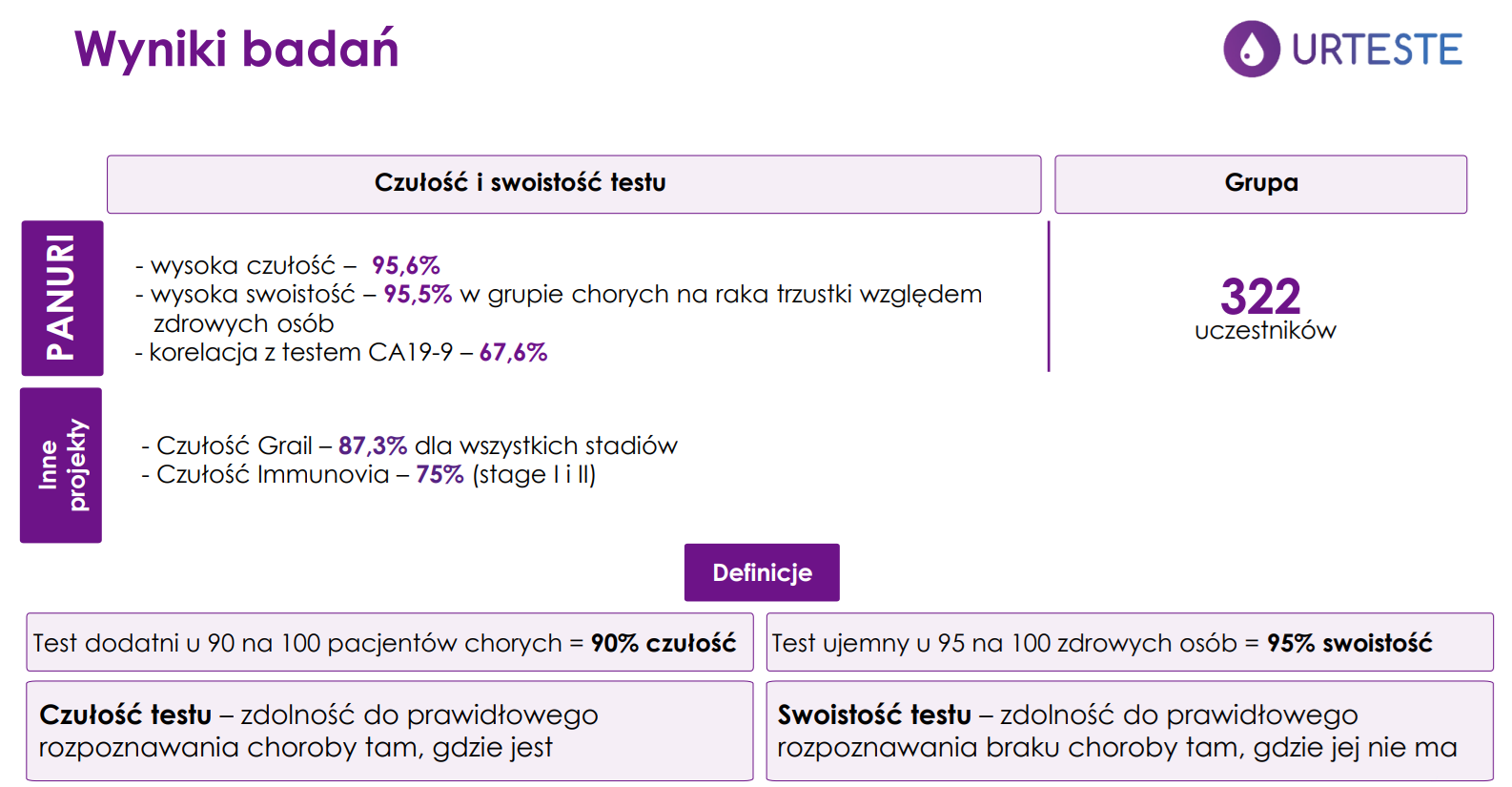
Zalety to potwierdzona wysoka czułość (95,6%) i swoistość (95,5%), szybki wyniki do 2 godzin i niski koszt. Także przewagą jest możliwość wykrywania wielu typów nowotworów i łatwa jednoznaczna interpretacja wyniku.
Na czym spółka się skupia, to jest rozwój kliniczny naszego testu. W tej chwili przygotowujemy badanie kliniczne, które planujemy przeprowadzić na terenie Stanów Zjednoczonych i Europy” – mówi - Grzegorz Stefański, współzałożyciel i prezes zarządu.
W ciągu ostatniego półrocza spółka odbyła dwa spotkania z FDA.
„FDA widzi bardzo dużą, poważną potrzebę wprowadzenia takiego testu na rynek USA, ponieważ obecnie na rynku takiego testu nie ma zaaprobowanego przez FDA” – mówi prezes.
„FDA wstępnie zaaprobowała pierwotny nasz plan badania. Natomiast bardzo mocno zaangażowała się w sam kształt tego testu i zaproponowała inne podejście do ukazania użyteczności tego testu oraz zaproponowała zmianę kształtu tego badania by podnieść jego użyteczność diagnostyczną” – dodaje.
Schemat badania klinicznego
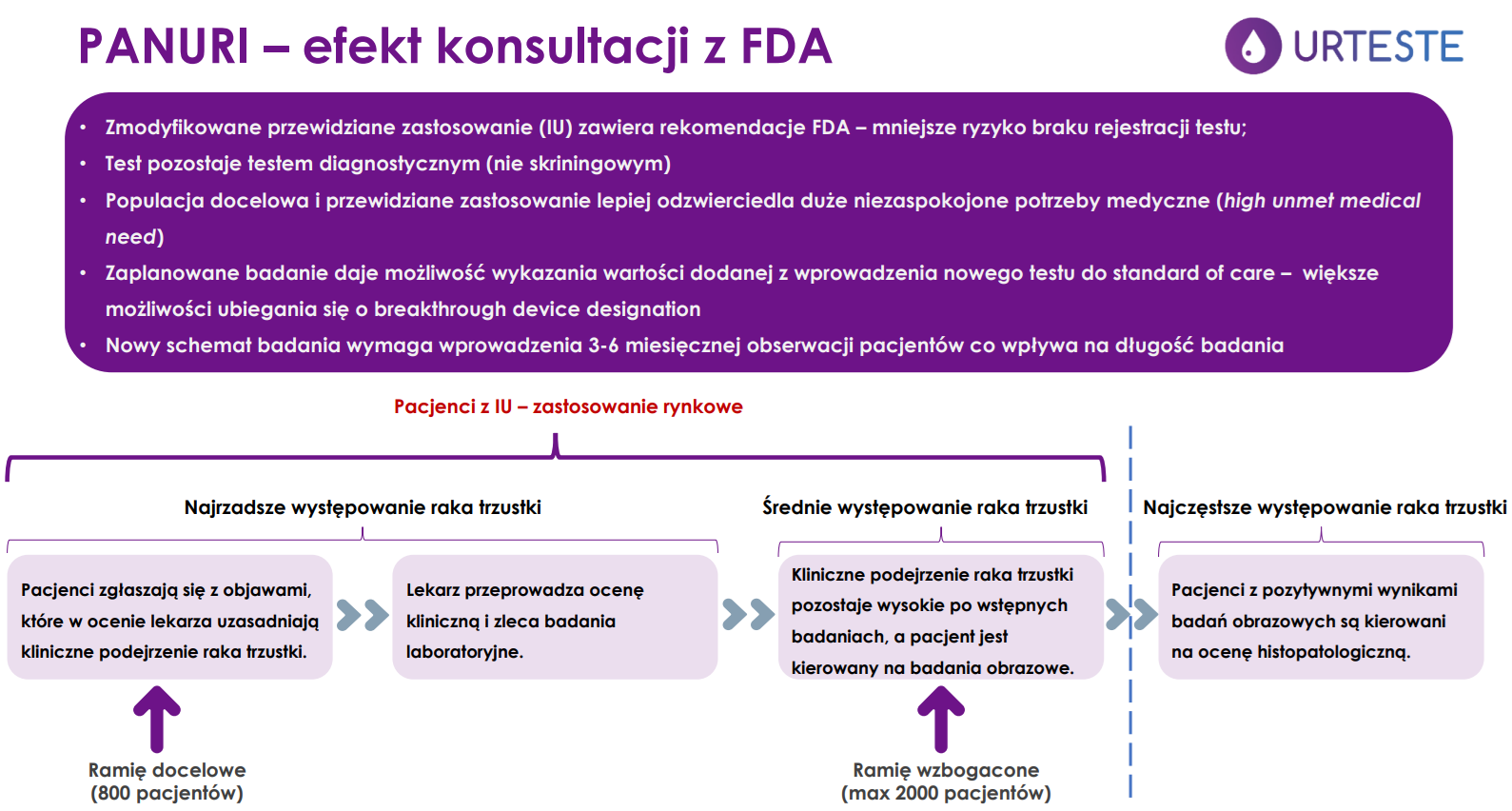
Test Panuri będzie zastosowany u dorosłych pacjentów z objawami raka trzustki. Schemat badania klinicznego będzie oparty o badanie dwóch grup (ramion). Ramię docelowe będzie badaniem na pacjentach z objawami klinicznymi – około 800 pacjentów.
Ze względu na to, że w tej grupie pacjentów szacujemy (z objawami - przyp. red.), że zaledwie 3% pacjentów ostatecznie będzie miało raka trzustki, z konieczności musimy dodać ramię wzbogacone, to będzie ok. 2000 pacjentów. To będą pacjenci, którzy już na podstawie objawów i dostępnych testów z krwi (…) będą skierowani na badania obrazowe z powodu podejrzenia raka trzustki” – wyjaśnia Grzegorz Stefański.
Głównym celem badania jest ocena skuteczności testu Panuri w wykrywaniu raka trzustki i wykazanie czułości i swoistości.
Po konsultacji z FDA, spółka zmodyfikowała badanie, by test mógł osiągnąć większą użyteczność kliniczną i tym samym zmniejszyć ryzyko braku rejestracji tego testu. Nowy schemat badania wymaga wprowadzenia 3-6 miesięcznej obserwacji pacjentów, co z kolei wpływa na długość badania. Daje jednak możliwość wykazania wartości dodanej z wprowadzenia nowego testu do „standard of care”, czyli zwiększa możliwości ubiegania się o tzw. „breaktrhrough device desgnation”.
„(...) breaktrhrough device desgnation pozwala na łatwiejszą komunikację z FDA, dwustronną komunikację, w całym procesie rejestracji produktu” – wyjaśnia prezes.
Spółka ma też już potwierdzone kolejne spotkanie z FDA zaplanowane na 24 stycznia.
Planowany start badania jest na pierwszy kwartał 2025 r. a jego zakończenie na 2026 r.
Urteste przyspiesza rozwój projektu NASTRO dzięki 11,5 mln zł dotacji z PARP
Finansowanie projektu
Spółka jest już w trakcje wyboru firmy CRO na przeprowadzenie badań klinicznych i ma zabezpieczony budżet na całe badanie.
„Na dzień dzisiejszy mamy zabezpieczony budżet na badanie. Jeśli nie wydarzy się nic nadzwyczajnego, powinniśmy w ramach posiadanych środków cele te osiągnąć” – zapewnia Tomasz Kostuch.
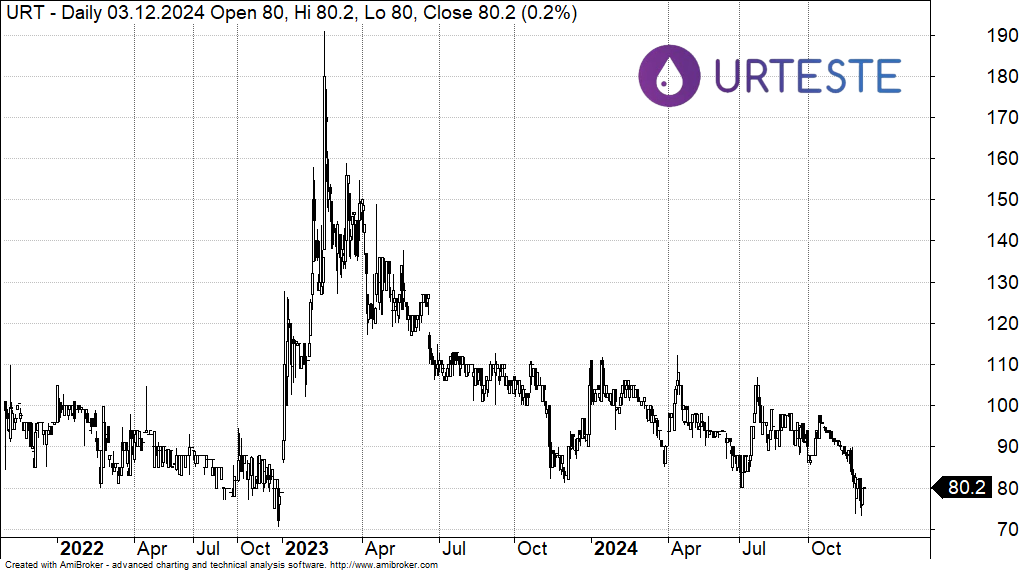
Kurs akcji Urteste od debiutu na GPW
Urteste prowadzi także projekt Nastro skierowany na wykrywanie raka piersi. Także w tym przypadku spółka ma zapewnione finansowanie. Otrzymała dofinansowanie 11,5 mln z PARP, przy czym całkowita wartość projektu jest szacowana na 20,8 mln zł.
Już są potencjalni partnerzy zainteresowani nawet wejściem w projekt na etapie badań klinicznych. Oddala się się więc ewentualna emisja akcji, której zarząd wolałby uniknąć. Tak więc dalszy rozwój badań Urteste ma być finansowany z dotacji i z partnerstwa m.in. z Clairfield.